En nuestro laboratorio estudiamos cómo los mecanismos epigenéticos median los efectos organizadores de las hormonas sexuales sobre el cerebro durante el período crítico perinatal. En particular, analizamos cómo la exposición temprana a testosterona regula procesos de desmetilación activa y reparación del ADN en la corteza prefrontal, y cómo estos mecanismos contribuyen al establecimiento de diferencias sexuales en la expresión génica asociada a trastornos del neurodesarrollo.
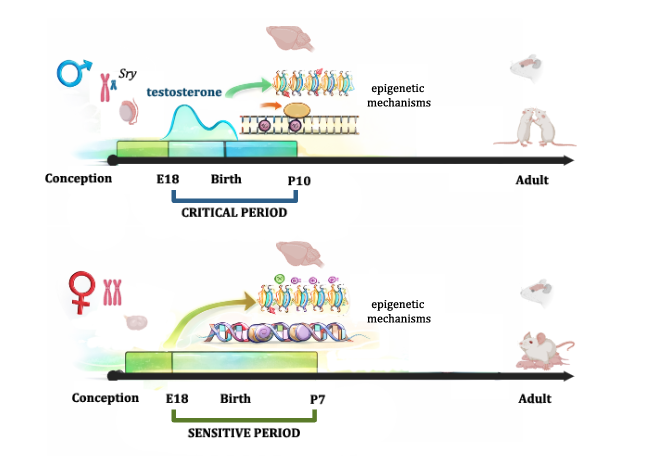
Diversos trastornos neuropsiquiátricos, como el trastorno del espectro autista y la esquizofrenia, se originan durante el desarrollo y presentan un sesgo sexual en su prevalencia, siendo más frecuentes en varones. Estas diferencias se vinculan, en gran medida, con la acción transitoria de hormonas gonadales durante una ventana crítica del desarrollo temprano, cuyos efectos organizadores son duraderos y generan una “memoria celular” en los circuitos neuronales.
En los últimos años, la metilación del ADN ha emergido como un mecanismo clave en la mediación de estos efectos. Lejos de ser estática, esta marca epigenética es altamente dinámica en el cerebro en desarrollo, lo que implica la existencia de procesos activos de desmetilación. En este contexto, las enzimas de la familia TET han sido identificadas como reguladores centrales de la remoción de metilación, además de establecer la hidroximetilación como una marca epigenética funcional relevante en el sistema nervioso.
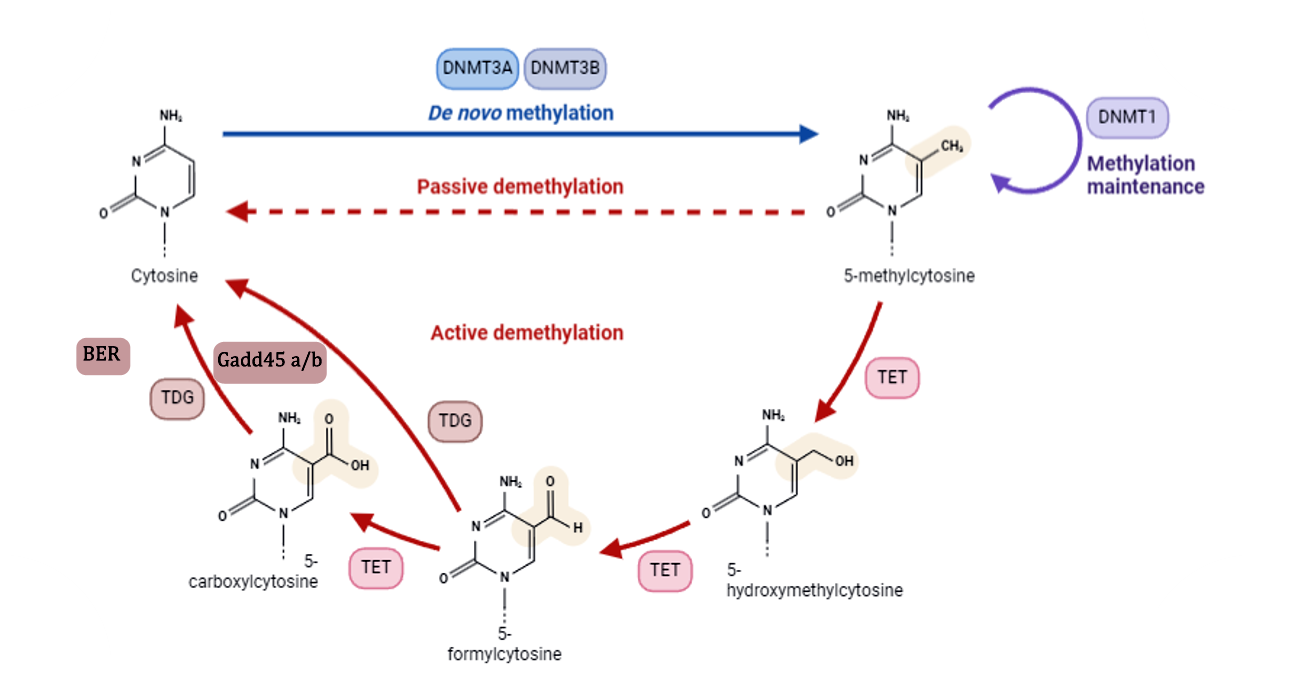
Nuestros estudios proponen que, durante el desarrollo, la regulación de genes sensibles a esteroides sexuales involucra ciclos dinámicos de metilación/desmetilación a nivel de regiones promotoras. Dado que los niveles globales de metilación del ADN son menores en machos en etapas tempranas, planteamos que el balance entre metilación y desmetilación podría estar desplazado hacia una mayor desmetilación en varones, generando una ventana de mayor sensibilidad a perturbaciones del desarrollo.
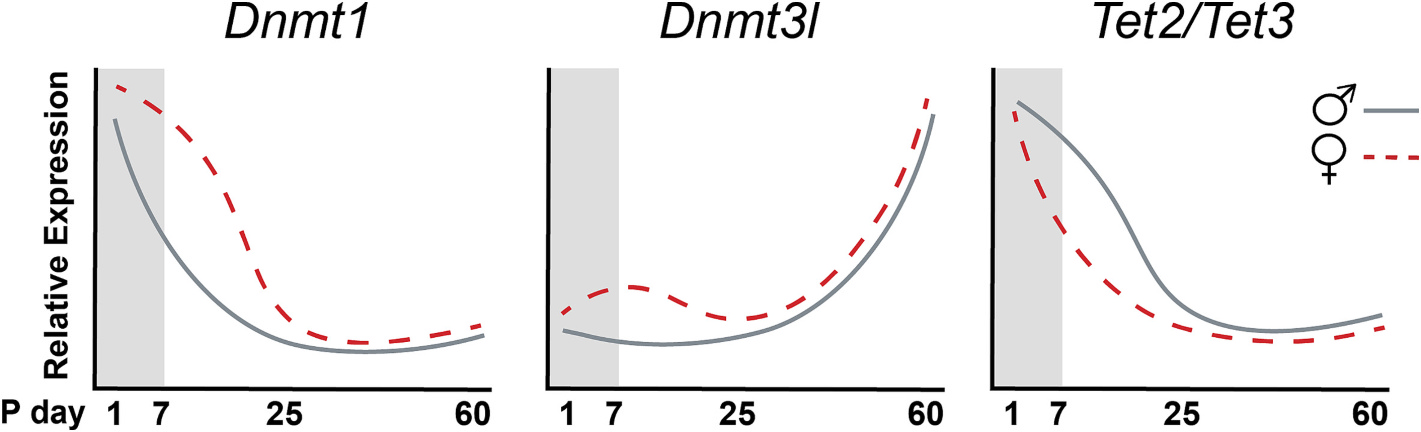
A largo plazo, buscamos integrar análisis epigenéticos, neurobiológicos y conductuales desde una perspectiva sexo-específica, con el objetivo de identificar mecanismos de vulnerabilidad diferencial y potenciales blancos para la prevención e intervención terapéutica en trastornos del neurodesarrollo.
FONDOS CONCURSABLES DE INVESTIGACIÓN
- 2025. IBRO-Wellcome, Neuroscience Capacity Accelerator for Mental Health (NCAMH) Understanding Sex Differences in PTSD Vulnerability Rol: Co-leader
- 2022-2023. PIBAA- CONICET. Rol de los esteroides gonadales en el control de la dinámica de metilación/demetilación del ADN durante el neurodesarrollo.
- 2022-2024. PICT-2020-SERIEA-00190. Fondo para la Investigación Científica y Tecnológica (FONCYT) Agencia Nacional de Promoción Científica y Tecnológica.
- 2021. Research Supplies for use in the applicant’s home laboratory. Committee for Aid and Education in Neurochemistry (CAEN) – International Society for Neurochemistry (ISN)
- 2019. Return Home Fellowship. International Brain Research Organization (IBRO).
PUBLICACIONES (ÚLTIMOS CINCO AÑOS)
- Pasquetta L, Dimundo J, Cisternas CD, Piovano J, Miranda-Morales RS. Parental care shapes anxiety-like behavior, oxytocin, social interaction, and ethanol sensitivity in adolescent C57BL/6J mice. Pharmacol Biochem Behav. 2026;263:174188. doi: 10.1016/j.pbb.2026.174188.
- Sosa C, Cabrera-Zapata LE, Cisternas CD, Arevalo MA, Cambiasso MJ. Sex chromosome-dependent epigenetic regulation underlies sex-specific H4 acetylation at the aromatase promoter in the developing mouse amygdala
Biol Sex Differ. 2026;17(1):57. doi: 10.1186/s13293-026-00854-4. - Castillo-Ruiz A, Cisternas CD, Sturgeon H, Forger NG. Birth triggers an inflammatory response in the neonatal periphery and brain. 2022 Brain Behav Immun. S0889-1591(22)00152-0. doi: 10.1016/j.bbi.2022.05.021
- Cabrera Zapata LE, Cisternas CD, Sosa C, Garcia-Segura LM, Arevalo MA, Cambiasso MJ. X-linked histone H3K27 demethylase Kdm6a regulates sexually dimorphic differentiation of hypothalamic neurons. Cell Mol Life Sci. 2021 78(21-22):7043-7060. doi: 10.1007/s00018-021-03945-0.
- Cortes LR, Cisternas CD, Cabahug INKV, Mason D, Ramlall EK, Castillo-Ruiz A, Forger NG. DNA methylation and demethylation underlie the sex difference in estrogen receptor alpha in the arcuate nucleus. Neuroendocrinology. 2021 doi: 10.1159/000519671.
- Hoffiz YC, Castillo-Ruiz A, Hall MAL, Hite TA, Gray JM, Cisternas CD, Cortes LR, Jacobs AJ, Forger NG. Birth elicits a conserved neuroendocrine response with implications for perinatal osmoregulation and neuronal cell death. Sci Rep. 11(1):2335. 2021 doi: 10.1038/s41598-021- 81511-1
- Cisternas CD, Cabrera Zapata LE, Mir FR, Scerbo MJ, Arevalo MA, Garcia-Segura LM, Cambiasso MJ. Estradiol-dependent axogenesis and Ngn3 expression are determined by XY sex chromosome complement in hypothalamic neurons. Sci Rep. 10(1):8223. 2020. doi: 10.1038/s41598-020-65183-x
- Cisternas CD, Cortes LR, Golynker I, Castillo-Ruiz A, Forger NG. Neonatal Inhibition of DNA Methylation Disrupts Testosterone-Dependent Masculinization of Neurochemical Phenotype. Endocrinology 161(1). 2020. doi: 10.1210/endocr/bqz022.
- Cisternas CD, Cortes LR, Bruggeman E, Yao B, Forger NG. Developmental changes and sex differences in the expression of DNA methylation and demethylation enzymes in hypothalamic regions of the mouse brain. Epigenetics, 15 (1-2), 72-84. 2020. doi: 10.1080/15592294.2019.1649528.
- Lista completa y actualizada disponible aquí.
EQUIPO DE TRABAJO DE LA DRA. CISTERNAS